- Autor Jason Gerald gerald@how-what-advice.com.
- Public 2023-12-16 11:06.
- Última modificación 2025-01-23 12:16.
La espectrofotometría es una técnica experimental utilizada para medir la concentración de un soluto en una solución particular calculando la cantidad de luz absorbida por esa sustancia. Esta técnica es muy útil porque ciertos compuestos también absorberán diferentes longitudes de onda de luz a diferentes intensidades. Al analizar la luz que atraviesa una solución, puede identificar los compuestos disueltos en la solución y sus concentraciones. La herramienta que se utiliza para analizar las soluciones con esta técnica en el laboratorio es un espectrofotómetro.
Paso
Parte 1 de 3: preparación de la muestra

Paso 1. Encienda el espectrofotómetro
La mayoría de los espectrofotómetros deben calentarse antes de que puedan dar mediciones precisas. Entonces, encienda la máquina y luego déjela reposar durante al menos 15 minutos antes de medir la muestra.
Utilice este tiempo para preparar la muestra

Paso 2. Limpiar la cubeta o el tubo de ensayo
En los laboratorios escolares, pueden estar disponibles tubos de ensayo desechables que no tienen que limpiarse primero. Sin embargo, si está utilizando una cubeta o un tubo de ensayo normal, asegúrese de limpiar el aparato a fondo antes de usarlo. Enjuague todas las cubetas con agua desionizada.
- Tenga cuidado al utilizar cubetas, ya que son bastante caras.
- Mientras usa la cubeta, no toque el lado por donde pasa la luz (generalmente el lado transparente del recipiente).
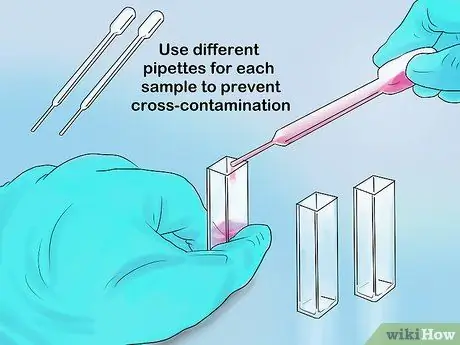
Paso 3. Vierta suficiente muestra en la cubeta
El volumen máximo de una parte de la cubeta es de 1 ml, mientras que el volumen máximo del tubo de ensayo es de 5 ml. Sus mediciones deben ser precisas siempre que la luz del espectrofotómetro pueda atravesar la muestra y no una parte vacía del recipiente.
Si está usando una pipeta para insertar muestras, use una punta nueva para cada muestra. De esa forma, se puede evitar la contaminación cruzada

Paso 4. Prepare la solución de control
Estas soluciones, que también se conocen como blancos o blancos, contienen solo el disolvente en la solución que se analiza. Por ejemplo, si tiene una muestra de sal disuelta en agua, la solución en blanco que necesita es agua. Si el agua que está usando es roja, también debe usar una solución en blanco roja. Utilice un recipiente similar para contener la solución en blanco en el mismo volumen que la muestra.

Paso 5. Limpie el exterior de la cubeta
Antes de insertar la cubeta en el espectrofotómetro, debe asegurarse de que esté limpia para evitar interferencias con las mediciones debido a partículas de polvo o impurezas. Utilice un paño sin pelusa para eliminar las gotas de agua o el polvo adherido al exterior de la cubeta.
Parte 2 de 3: Experimentar

Paso 1. Determine y ajuste la longitud de onda de la luz para analizar la muestra
Utilice una única longitud de onda de luz (haz monocromático) para aumentar la eficacia de la medición. Elija el color de la luz que puede ser absorbido por el contenido químico que se cree que se disuelve en la muestra de prueba. Configure la longitud de onda de acuerdo con las especificaciones del espectrofotómetro que esté utilizando.
- En los laboratorios escolares, estas longitudes de onda generalmente se darán en las instrucciones experimentales.
- Debido a que la muestra reflejará toda la luz visible, la longitud de onda del color de la luz experimental suele ser siempre diferente del color de la muestra.
- Un objeto tiene un color determinado porque refleja una longitud de onda determinada y absorbe todos los demás colores. La hierba parece verde porque la clorofila que contiene refleja el verde y absorbe otros colores.
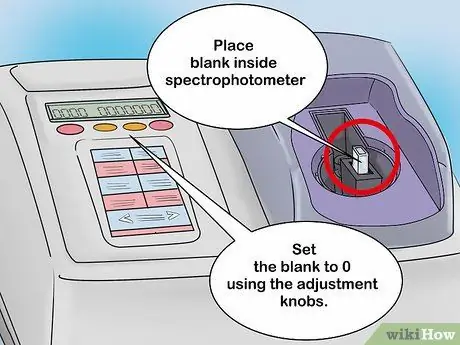
Paso 2. Calibre el espectrofotómetro con una solución en blanco
Coloque la solución en blanco en el soporte de la cubeta y cierre el espectrofotómetro. En la pantalla del espectrofotómetro analógico, hay una aguja que se moverá según la intensidad de la detección de luz. Una vez que se inserta la solución en blanco, la aguja debe moverse hacia la derecha. Registre este valor en caso de que lo necesite más adelante. Deje que la solución en blanco permanezca en el espectrofotómetro, luego deslice la aguja a cero usando la perilla de ajuste.
- Los espectrofotómetros digitales también se pueden calibrar de la misma manera. Sin embargo, esta herramienta está equipada con una pantalla digital. Establezca la lectura de la solución en blanco en 0 con la perilla de control.
- Incluso si se retira la solución en blanco del espectrofotómetro, la calibración seguirá siendo válida. Por lo tanto, cuando mida toda la muestra, la absorbancia del blanco se reducirá automáticamente.

Paso 3. Retire el blanco y pruebe los resultados de la calibración del espectrofotómetro
Incluso después de retirar la solución en blanco del espectrofotómetro, la aguja o el número en la pantalla aún debe leer 0. Vuelva a colocar la solución en blanco en el espectrofotómetro y asegúrese de que la lectura no cambie. Si el espectrofotómetro está calibrado correctamente con una solución en blanco, el resultado en la pantalla aún debería ser 0.
- Si la aguja o el número en la pantalla no lee 0, repita los pasos de calibración con una solución en blanco.
- Si el problema persiste, busque ayuda o pídale a alguien que revise el espectrofotómetro.

Paso 4. Mida la absorbancia de la muestra
Retire la solución en blanco e inserte la muestra en el espectrofotómetro. Espere unos 10 segundos para que las manecillas se estabilicen o los números en la pantalla digital dejen de cambiar. Registre el porcentaje de transmitancia y / o absorbancia de la muestra.
- Cuanta más luz pasa, menos luz se absorbe. Por lo general, debe registrar el valor de absorbancia de la muestra, que generalmente se expresa como un número decimal, por ejemplo, 0,43.
- Repita la medición de cada muestra al menos tres veces y luego calcule el promedio. De esa forma, los resultados que obtenga serán más precisos.

Paso 5. Repita el experimento con diferentes longitudes de onda de luz
Su muestra puede contener varios compuestos que tienen diferentes absorbancias según la longitud de onda de la luz. Para reducir la incertidumbre, repita las mediciones de la muestra a intervalos de longitud de onda de 25 nm en todo el espectro de luz. De esta forma, puede detectar otros productos químicos disueltos en la muestra.
Parte 3 de 3: Análisis de datos de absorbancia

Paso 1. Calcule la transmitancia y absorbancia de la muestra
La transmitancia es la cantidad de luz que puede atravesar la muestra y llegar al espectrofotómetro. Mientras tanto, la absorbancia es la cantidad de luz que absorbe uno de los productos químicos disueltos en la muestra. Hay muchos espectrofotómetros modernos que dan salida en forma de transmitancia y absorbancia. Sin embargo, si obtiene un valor de intensidad de luz, también puede calcular estos dos valores usted mismo.
- La transmitancia (T) se puede determinar dividiendo la intensidad de la luz que pasa a través de la solución de muestra por la cantidad de luz que pasa a través de la solución en blanco. Este valor generalmente se expresa como un número decimal o un porcentaje. T = yo / yo0, donde yo es la intensidad de la muestra y yo0 es la intensidad en blanco.
- La absorbancia (A) se expresa como una transmitancia de logaritmo (exponente) de base 10 negativa: A = -log10T. Entonces, si T = 0, 1, A = 1 (0, 1 es 10 elevado a -1). Esto significa que se pasa el 10% de la luz, mientras que se absorbe el 90%. Mientras tanto, si T = 0.01, A = 2 (0.01 es 10 elevado a -2). Esto significa que la luz que se transmite es del 0,1%.
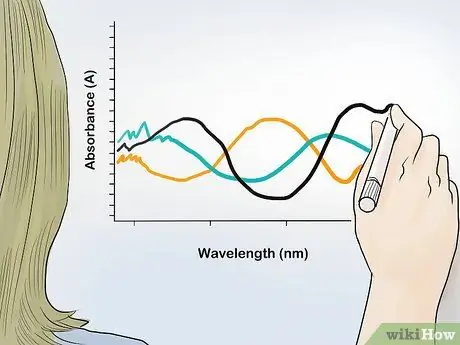
Paso 2. Grafique el valor de absorbancia en función de la longitud de onda
Exprese el valor de absorbancia como eje y y la longitud de onda como eje x. A partir de los puntos de todos los resultados de absorbancia en cada longitud de onda, obtendrá el espectro de absorbancia de la muestra e identificará el contenido del compuesto y su proporción en la muestra.
Los espectros de absorbancia suelen tener picos en determinadas longitudes de onda. Estas longitudes de onda máximas le permiten identificar compuestos específicos
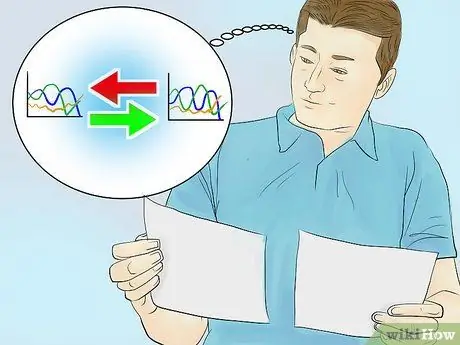
Paso 3. Compare su espectro de absorbancia con una gráfica de un compuesto conocido
Cada compuesto tiene un espectro de absorbancia único y siempre tiene la misma longitud de onda máxima en cada medición. Al comparar el gráfico que obtiene con un gráfico de un determinado compuesto conocido, puede identificar el contenido de soluto en la solución de muestra.






